 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
知识点二 无机含氧酸酸性的考查3.下列有关含氧酸的说法中正确的是()
A.元素的非金属性越强,其含氧酸的酸性就越强
B.含氧酸中有多少个氢原子,就属于几元酸
C.同一元素的不同含氧酸,非羟基氧越多,该酸的酸性越强
D.含氧酸中,中心原子的化合价越高,其氧化性一定越强
 答案
答案
C、同一元素的不同含氧酸,非羟基氧越多,该酸的酸性越强
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.元素的非金属性越强,其含氧酸的酸性就越强
B.含氧酸中有多少个氢原子,就属于几元酸
C.同一元素的不同含氧酸,非羟基氧越多,该酸的酸性越强
D.含氧酸中,中心原子的化合价越高,其氧化性一定越强
 答案
答案
C、同一元素的不同含氧酸,非羟基氧越多,该酸的酸性越强
 更多“知识点二 无机含氧酸酸性的考查3.下列有关含氧酸的说法中正确的是()”相关的问题
更多“知识点二 无机含氧酸酸性的考查3.下列有关含氧酸的说法中正确的是()”相关的问题
第1题
A.无机含氧酸分子中含有几个氢原子,它就属于几元酸
B.同周期非金属元素的氧化物对应水化物的酸性从左到右依次增强
C.同一元素的含氧酸,该元素的化合价越高,酸性越强
D.H3PO4和H2CO3分子中非羟基氧的个数均为1,它们的酸性相近,均为中强酸
第5题
简要回答下列问题:
(1)拟将下列离子转化为碳酸正盐,试说明怎样选择沉淀剂,并写出反应方程式:
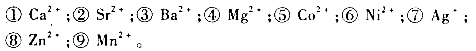
(2)从二氧化硅氯化制备SiCl4,需要和焦炭共热进行反应的耦合:
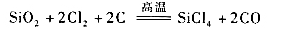
而用HF对二氧化硅进行氟化制备SiF4则不需要反应的耦合:
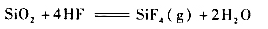
(3)Pb与稀盐酸反应,速率很慢且反应会停止;但与浓盐酸作用时,反应容易进行。试给出合理解释。
(4)从H3BO3显酸性的机理去说明为什么H3BO3是一元弱酸。
(5)试解释下列无机含氧酸的氧化性由强到弱的原因:
HClO4>H2SO4>H3PO4>H2SiO3
(6)为什么硅不与氧化性酸反应,但又可溶于HNO3及HF混合溶液中?
(7)用平面图示的方法表示单聚硅酸根SiO44-,焦硅酸根Si2O74-,链三聚硅酸根和环六聚硅酸根。写出链n聚和环n聚多硅酸根的化学式。
(8)画简图表示乙硼烷的结构,并说明其中3中心2电子键的形成过程。
(9)硼砂Na2[B4O5(OH)4]·8H2O是四硼酸的钠盐。试说明通常将硼砂的化学式写成Na2B4O7原因。为什么硼砂溶于水形成缓冲溶液?试计算其pH。
(10)三氟化硼分子是单聚体BF3,同样属于缺电子结构的乙硼烷分子却是B2H6。或者说是二聚的BH3。从结构角度如何解释这种现象?
(11)BiI5和PbI4均不能稳定存在,却有TU3存在,试说明其原因。
(12)试比较乙硼烷、烷烃、甲硅烷三者的热稳定性,写出其受热分解的化学反应方程式。
第6题
A.概括与抽象
B.分类与比较
C.分析与综合
D.系统化与具体化
第7题
A.HClO3
B.H2SeO3
C.H2BO2
D.HMnO4
第8题
A.还原性强弱: S(2-) < I- < Cl-
B.半径大小: S(2-) > Cl- > K+ > Ca(2+)
C.核外电子排布相同的微粒化学性质相同
D.同主族元素含氧酸的酸性随核电荷数的增加而减弱
第9题
A.第一电离能:Y小于X
B.气态氢化物的稳定性:HmY小于HnX
C.最高价含氧酸的酸性:X对应的酸性强于Y对应的
D.X和Y形成化合物时,X显负价,Y显正价
第10题
A.从受力和能量角度分析带电粒子的运动是考试的重点
B.高考中会用综合题考查,不会考选择
C.电势能和电势,带电粒子在电场中的运动,电势差都是静电场很重要的知识点
第11题
A.从两性金属氧化矿或冶金中间产品中浸出有色金属
B.从碱性金属氧化渣里浸出有色金属
C.分解含氧酸盐矿
D.从精矿或冶金中间产品中除去酸性或两性杂质