 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
固溶体晶体中的溶质原子属于()。
A.面缺陷
B.体缺陷
C.点缺陷
D.线缺陷
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.面缺陷
B.体缺陷
C.点缺陷
D.线缺陷
 答案
答案
 更多“固溶体晶体中的溶质原子属于()。”相关的问题
更多“固溶体晶体中的溶质原子属于()。”相关的问题
第2题
A.固溶体会破坏原子排列规律,使金属的强度降低
B.置换固溶体又称为无限固溶体
C.金属化合物能使合金的强度、硬度提高,称为弥散强化
D.Fe3C(渗碳体)属于间隙化合物
第3题
A、组成铁碳合金的组元只有Fe、C
B、Pb-Sn合金的固态相结构只有一种
C、固溶体会破坏原子排列,使金属的强度、硬度提高
D、Fe3C(渗碳体)属于间隙固溶体
第4题
已知NaCl的晶体结构如图C.17.1所示,它属于立方晶系,Oh点群。晶胞参数=564.0pm。
(I)写出通过晶胞中心的点对称元素。
(2)根据Na+和Cl-的离子半径值,了解在这结构中负离子是否接触?这种结构的稳定性如何?
(3)试计算NaCl晶体的密度D。
(4)将图C.17.1晶胞中顶角上的Na+和中心的Cl-除去,将Na+换成Nb2+,Cl-换得O2-即得NbO晶胞,试画出NbO的晶胞和其中原子簇的结构;已知晶跑参数 =421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
=421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
(5)将图C.17.1晶胞中面心和体心的原子除去,顶角上的Na+换成U6+,棱上的Cl-换成O2-,得UO3的晶体结构,立方晶胞参数a=415.6pm。试画出UO3晶胞的结构;写出通过晶胞中心点的点对称元素和点群;计算晶体的密度,计算U6+的离子半径(U的相对原子质量为238.0);画出由处在12条棱上的02-组成的立方八面体的图形;计算该多面体的自由孔径。
第7题
铝中加入的合金元素溶解在铝晶格中,使晶格发生畸变,造成铝基体强化,这种结构叫以铝为基体的()。
A.化合物
B.固溶体
C.金属间化合物
D.晶体
第8题
第10题
A.电子在整个分子范围内运动,不再属于某一特定原子
B.反键分子轨道的能量比所有成键分子轨道高,此当反键分子轨道上有电子时,分子不稳定
C.分子轨道是不同原子的原子轨道线性组合面成,杂化轨道是同一原子的原子轨道组合而成
D.只有符合对称性匹配、能量相近和最大重叠原则的原子轨道才能有效地组合成分子轨道
第11题
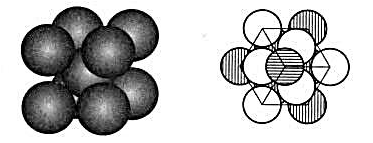
(1)试计算金属晶体中钾原子的空间占有率;
(2)试计算金属晶体中铂原子的空间占有率;
(3)已知铂的相对原子质量为195.08,若金属铂的立方晶胞的边长a=392.3pm,试计算每立方厘米金属铂的质量。