 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某温度下,反应的速率常数k=8.8×10-2dm6·mol-2·s-1。已知此反应对O2⌘
某温度下,反应
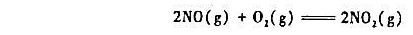
的速率常数k=8.8×10-2dm6·mol-2·s-1。已知此反应对O2是1级的,当两种反应物浓度都是 0.050mol-1·dm-3时,此反应的反应速率是多少?
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某温度下,反应
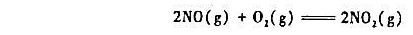
的速率常数k=8.8×10-2dm6·mol-2·s-1。已知此反应对O2是1级的,当两种反应物浓度都是 0.050mol-1·dm-3时,此反应的反应速率是多少?
 答案
答案
 更多“某温度下,反应的速率常数k=8.8×10-2dm6·mol-2·s-1。已知此反应对O2⌘”相关的问题
更多“某温度下,反应的速率常数k=8.8×10-2dm6·mol-2·s-1。已知此反应对O2⌘”相关的问题
第1题
有关反应速率的叙述中错误的是()。
A.绝大多数反应的反应速率随温度升高而增大
B.活化能大的反应速率也大
C.速率常数大的反应速率大
D.对于相同温度下的不同的反应,活化能越大,速率常数随温度的变化率越大
第2题
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算
(1)400K时,反应的速率为原来的多少倍?
(2)温度由1000K升高到1100K时,反应速率为1000K时的多少倍?
第4题
在酸性溶液中,反应 的速率方程为v=
的速率方程为v=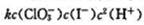 .在下列三项中,影响反应速率的因素有(),影响速率常数的因素为().
.在下列三项中,影响反应速率的因素有(),影响速率常数的因素为().
①在反应中加人水;②在反应溶液中加入氨;③反应溶液从20℃加热到35℃.
第5题
250K时化学反应A+2B=2C速率和浓度的关系如下:

(1)写出反应的速率方程,并指出反应指数.
(2)求该反应的速率常数.
(3)求出当c(A)=0.010mol·L-1,c(B)=0.020mol·L-1时的反应速率.
第6题
660K时的反应2NO+02→2NO2NO和O2的初始浓度c(NO)和c(O2)及反应初始速率v的实验数据为:
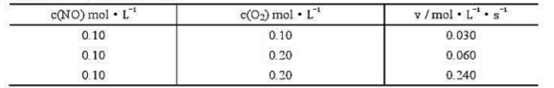
(1)写出反应的速率方程
(2)求反应的级数和速率常数
(3)求c(NO)=c(O2)=0.15molL-1时的反应速率。
第7题
A.反应速率常数单位为[时间]-1
B.反应物浓度的对数与反应时间呈线型关系
C.半衰期与反应物初始浓度无关
D.消耗75%反应物所需时间为消耗50%反应物所需时间的两倍
第8题
某温度下,反应 的实验数据如下表所示:
的实验数据如下表所示:
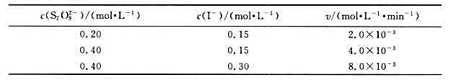
则该反应的速率方程是()。
A、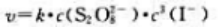
B、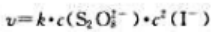
C、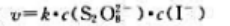
D、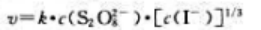
第10题
A.反应的活化能越大,在一定的温度下,反应速度也越快
B.反应的活化能越大,在一定的温度下,反应速度也越慢
C.凡是活化能大的反应,只能在高温下进行
D.某反应体系的温度一定时,当反应物的一部分活化分子全部反应后,反应就停止
第11题
A.11
B.10
C.10.78
D.8.8