 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
若往含有0.10mol·dm-3ZnCl2和0.10mol·dm-3CuCl2的混合溶液中通入H2S至饱和,按下式计算溶液中Zn2+的浓度:Zn2
若往含有0.10mol·dm-3ZnCl2和0.10mol·dm-3CuCl2的混合溶液中通入H2S至饱和,按下式计算溶液中Zn2+的浓度:Zn2++H2S====ZnS+2H+。
(已知

H2S:

 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
若往含有0.10mol·dm-3ZnCl2和0.10mol·dm-3CuCl2的混合溶液中通入H2S至饱和,按下式计算溶液中Zn2+的浓度:Zn2++H2S====ZnS+2H+。
(已知

H2S:

 答案
答案
 更多“若往含有0.10mol·dm-3ZnCl2和0.10mol·dm-3CuCl2的混合溶液中通入H2S至饱和,按下式计算溶液中Zn2+的浓度:Zn2”相关的问题
更多“若往含有0.10mol·dm-3ZnCl2和0.10mol·dm-3CuCl2的混合溶液中通入H2S至饱和,按下式计算溶液中Zn2+的浓度:Zn2”相关的问题
第2题
A.0.05mol
B.0.10mol
C.0.15mol
D.1.0mol
第3题
A.X中一定不存在Fe2O3、MnO2
B.X中一定含有Fe、CuO和K2CO3
C.往溶液Z中加入AgNO3溶液,若产生白色沉淀,则Z中含NaCl
D.取溶液W,加少盐NaOH溶液,肯定产生沉淀
第4题
用0.10mol·L-1NaOH溶液滴定同浓度的HAc溶液时,若用甲基橙为指示剂(终点时pH=4.0),问终点时未被中和的HAc是多少?
第5题
将等体积的0.40mol/L Fe2+溶液和0.10mol/L Ce4+溶液相混合,若溶液中H2SO4浓度为0.5mol/L,问反应达平衡后,Ce4+的浓度是多少?
第9题
往含有0.1mol/L的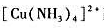 配离子溶液中,加入氨水,使溶液中NH3浓度为1.0mol/L,请计算达到平衡时溶液中Cu2+离子浓度为多少?已知
配离子溶液中,加入氨水,使溶液中NH3浓度为1.0mol/L,请计算达到平衡时溶液中Cu2+离子浓度为多少?已知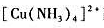 的
的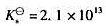
第10题
A.在乙酸乙酯粗产品中加入含酚酞的氢氧化钠溶液,振荡液体分层,下层溶液变浅红色或无色乙酸乙酯粗产品中一定含有乙酸
B.在苯中加溴化铁和溴水 剧烈反应且颜色变浅苯与溴发生取代反应
C.往植物油中滴加溴的四氯化碳溶液溶液颜色消失 植物油含有酯基
D.往酸性高锰酸钾溶液中滴加葡萄糖溶液,振荡、静置 紫红色溶液逐渐变浅、最终褪色葡萄糖具有还原性
第11题
有下列原电池:
(-)Cd|cdSO4(1.0mol·L-1)||CuSO4(1.0mol·L-1)l Cu()
若往CdSO4溶液中加入少量Na2S溶液,或往cuSO4溶液中加入少量CuSO4·5H2O晶体,都会使原电池的电动势变小。( )