 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将锌片置于PH=2,0.01mol/LZnCl2溶液中,该锌片能否被腐蚀?为什么?
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“将锌片置于PH=2,0.01mol/LZnCl2溶液中,该锌片能否被腐蚀?为什么?”相关的问题
更多“将锌片置于PH=2,0.01mol/LZnCl2溶液中,该锌片能否被腐蚀?为什么?”相关的问题
第1题
A.锌片做负极,锌发生还原反应
B.铜片做正极,铜得电子
C.溶液中的PH值增大
D.锌片、铜片同时有气泡冒出,说明锌片不纯
第2题
(1)写出原电池符号、电池反应式;
(2)查标准电极电势表,求该原电池的标准电动势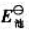 ;
;
(3)当电池反应进行到c(Cu2+)=1.0mol·dm-3时,试计算原电池的电动势E池。
第3题
A.通过对比实验说明西红柿汁是电解质溶液而橘子汁是非电解质溶液
B.通过对比实验得出西红柿汁:pH<7,橘子汁:pH>7
C.用橘子探究原电池工作原理的实验不可能获得成功
D.通过对比实验说明构成原电池条件之一是两极要和电解质溶液接触并形成闭合回路
第4题
A.1/2· (10-8+10-10) mol/L
B.(10-8+10-10) mol/L
C.(1.0×10-14+5×10-5)mol/L
D.2×10-10 mol/L
第5题
A.锌片是正极,铜片上有气泡产生
B.电流方向是从锌片流向铜片
C.溶液中的阳离子向正极移动,阴离子向负极移动
D.电解质液的PH值逐渐减少
第6题
A.若混合后溶液pH=7,则c(NH4+)=c(Cl-)
B.若a=2,则c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C.若a=0.5,则c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D.若混合后溶液满足c(H+)=c(OH-)+c(NH3·H2O),则可推出a=1
第7题
A.=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)=mol/L
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
第8题
A.等体积混合浓度均为0.2 mol·L-1的AgNO3溶液和CH3COONa溶液一定产生CH3COOAg沉淀
B.将0.001 mol·L-1的AgNO3溶液滴入0.001 mol·L-1的KCl和0.001 mol·L-1的K2CrO4溶液中先产生Ag2CrO4沉淀
C.在Mg2+为0.121 mol·L-1的溶液中要产生Mg(OH)2沉淀,溶液的pH至少要控制在9以上
D.向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)变大
第10题
A.铁片产生气体速率快,说明铁比锌活泼
B.锌片产生气体速率快,说明锌比铁活泼
C.铁片产生气体速率慢,说明铁比锌活泼
D.锌片产生气体速率慢,说明锌比铁活泼
第11题
A.-0.762V
B.-0.801V
C.-0.821V
D.-0.703V