 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一元弱酸HB的电离常数Ka()与其共轭碱B的 电离常数Kb(B‾)在水溶液中的关系是
A.Ka(HB)= Kb(B‾)
B.Ka(HB)Kb(B‾)=1
C.Ka(HB) Kb(B‾)= Kw
D.Ka(HB)/Kb(B‾)= Kw
 答案
答案
B、Ka(HB)Kb(B‾)=1
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Ka(HB)= Kb(B‾)
B.Ka(HB)Kb(B‾)=1
C.Ka(HB) Kb(B‾)= Kw
D.Ka(HB)/Kb(B‾)= Kw
 答案
答案
B、Ka(HB)Kb(B‾)=1
 更多“一元弱酸HB的电离常数Ka()与其共轭碱B的 电离常数Kb(B‾)在水溶液中的关系是”相关的问题
更多“一元弱酸HB的电离常数Ka()与其共轭碱B的 电离常数Kb(B‾)在水溶液中的关系是”相关的问题
第1题
已知0.1mol·L-1一元弱酸HB的pH=3.0,问其等浓度的共轭碱NaB的pH值为多少?(已知Kac>10Kw,且c/Ka>100。)
第2题
已知弱酸 的离解常数为Ka=5.6×10-10,则其共轭碱的pKb为()
A.4.74
B.3.74
C.5.60
D.9.26
第5题
已知0.10 mol·L-1—元弱酸HB溶液的pH=3.5,则0.10 mol·L-1共轭碱NaB溶液的pH是()。
A.10.5
B.10.0
C.9
D.9.5
第6题
由一元弱酸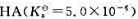 和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
第7题
欲配制pH=3的缓冲溶液,已知有下列物质的Ka数值:
(1) HCOOH Ka=1.77×10-4;
(2) HAc Ka=1.76×10-5;
(3) NH4+Ka=5.65×10-10。
问选择哪一种弱酸及其共轭碱较合适?