 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列反应的离子方程式书写正确的是()。
A.CO2通入NaAlO2溶液中AlO+CO2+H2O===Al(OH)3↓+CO
B.Al2O3与过量氨水Al2O3+6NH3•H2O===2Al3++6NH
C.向AlCl3溶液中加入过量NaOH溶液Al3++3OH-===Al(OH)3↓
D.向AlCl3溶液中滴入过量的氨水Al3++3NH3•H2O===Al(OH)3↓+3NH
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.CO2通入NaAlO2溶液中AlO+CO2+H2O===Al(OH)3↓+CO
B.Al2O3与过量氨水Al2O3+6NH3•H2O===2Al3++6NH
C.向AlCl3溶液中加入过量NaOH溶液Al3++3OH-===Al(OH)3↓
D.向AlCl3溶液中滴入过量的氨水Al3++3NH3•H2O===Al(OH)3↓+3NH
 答案
答案
 更多“下列反应的离子方程式书写正确的是()。”相关的问题
更多“下列反应的离子方程式书写正确的是()。”相关的问题
第2题
A.MnO4—+S2-+4H+=MnO2+S
B.2MnO4—+5S2-+16H+=2Mn2++5S↓+8H2O↑+2H2O
C.MnO4—+S2-+4H+=Mn2++SO2
D.2MnO4—+S2-+4H+=2MnO4—+SO2↑+2H2O
第5题
简要回答下列问题:
(1)拟将下列离子转化为碳酸正盐,试说明怎样选择沉淀剂,并写出反应方程式:
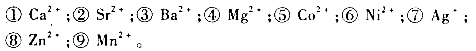
(2)从二氧化硅氯化制备SiCl4,需要和焦炭共热进行反应的耦合:
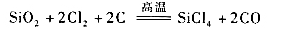
而用HF对二氧化硅进行氟化制备SiF4则不需要反应的耦合:
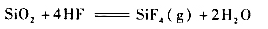
(3)Pb与稀盐酸反应,速率很慢且反应会停止;但与浓盐酸作用时,反应容易进行。试给出合理解释。
(4)从H3BO3显酸性的机理去说明为什么H3BO3是一元弱酸。
(5)试解释下列无机含氧酸的氧化性由强到弱的原因:
HClO4>H2SO4>H3PO4>H2SiO3
(6)为什么硅不与氧化性酸反应,但又可溶于HNO3及HF混合溶液中?
(7)用平面图示的方法表示单聚硅酸根SiO44-,焦硅酸根Si2O74-,链三聚硅酸根和环六聚硅酸根。写出链n聚和环n聚多硅酸根的化学式。
(8)画简图表示乙硼烷的结构,并说明其中3中心2电子键的形成过程。
(9)硼砂Na2[B4O5(OH)4]·8H2O是四硼酸的钠盐。试说明通常将硼砂的化学式写成Na2B4O7原因。为什么硼砂溶于水形成缓冲溶液?试计算其pH。
(10)三氟化硼分子是单聚体BF3,同样属于缺电子结构的乙硼烷分子却是B2H6。或者说是二聚的BH3。从结构角度如何解释这种现象?
(11)BiI5和PbI4均不能稳定存在,却有TU3存在,试说明其原因。
(12)试比较乙硼烷、烷烃、甲硅烷三者的热稳定性,写出其受热分解的化学反应方程式。
第8题
第10题
某氮肥厂氨氮废水中的氮元素多以NH和NH3·H2O的形式存在,该废水的处理流程如下:![]()
问题一、过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。
①用离子方程式表示加NaOH溶液的作用:()。
②用化学平衡原理解释通空气的目的:()。
问题二、过程Ⅱ:在微生物作用的条件下,NH经过两步反应被氧化成NO。两步反应的能量变化示意图如下:
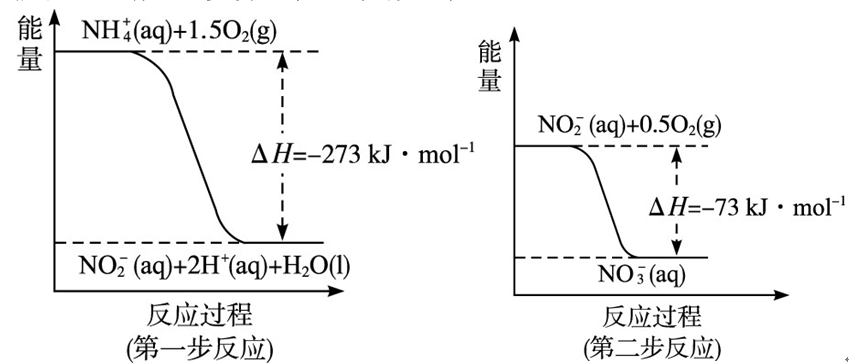
①第一步反应是()反应(选填“放热”或“吸热”),判断依据是()。
②1molNH(aq)全部氧化成NO(aq)的热化学方程式是()。
问题三、过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3复原成N2。假设该反应消耗32gCH3OH转移6mol电子,则参加反应的复原剂和氧化剂的物质的量之比是()。
第11题
下列反应方程式配平的是 ________ 。
A.K2Cr2O7+K2SO3+4H2SO4→Cr2(SO4)3+2K2SO4+4H2O
B.FeS+4HNO3→Fe(NO3)3+S↓+NO↑+H2O
C.MnS+8HNO3(浓)→MnSO4+8NO2↑+4H2O