 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知空气—锌电池的电极反应为锌片:Zn+2OH-— 2e-=ZnO+H2O;碳棒:0.5O2+H2O+2e-=2OH-,据此判断,锌片是()
A.正极并被还原
B.正极并被氧化
C.负极并被还原
D.负极并被氧化
 答案
答案
D、负极并被氧化
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.正极并被还原
B.正极并被氧化
C.负极并被还原
D.负极并被氧化
 答案
答案
D、负极并被氧化
 更多“已知空气—锌电池的电极反应为锌片:Zn+2OH-— 2e-=ZnO+H2O;碳棒:0.5O2+H2O+2e-=2OH-,据此判断,锌片是()”相关的问题
更多“已知空气—锌电池的电极反应为锌片:Zn+2OH-— 2e-=ZnO+H2O;碳棒:0.5O2+H2O+2e-=2OH-,据此判断,锌片是()”相关的问题
第1题
A.-0.762V
B.-0.801V
C.-0.821V
D.-0.703V
第2题
A.通CO的一极是电池的正极
B.负极发生的电极反应是O2+2CO2+4e-=2CO32-
C.负极发生的电极反应是CO+CO32--2e-=2CO2
D.正极发生氧化反应
第3题
A.电池工作时,COeq \o\al(2-,3)向负极移动
B.电池放电时,电子经外电路由通氧气的正极流向通氢气的负极
C.正极的电极反应为4OH--2e-===O2↑+2H2O
D.通氧气的电极为正极,发生氧化反应
第4题
丙烷燃料电池的电极反应为
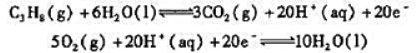
(1)指出正极反应和负极反应;
(2)写出电池反应方程式;
(3)计算25℃下丙烷燃料电池的标准电动势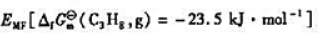
第5题
我国科学家研发了一种室温下“可呼吸”的Na-CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO+4Na⇋2Na2CO3+C。下列说法错误的是()。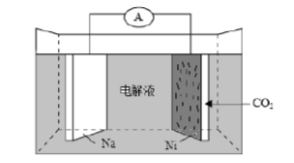
A.放电时,ClO4-向负极移动
B.充电时释放CO2,放电时吸收CO2
C.放电时,正极反应为:3CO2+4e-=2CO32-+C
D.充电时,正极反应为:Na++e-=Na
第6题
将反应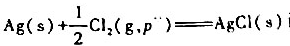 设计成原电池.已知25°C;时,
设计成原电池.已知25°C;时,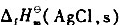 =-127.07kJ.mol-1.
=-127.07kJ.mol-1.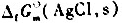 =-109.79kJ.mol-1,标准电极电势
=-109.79kJ.mol-1,标准电极电势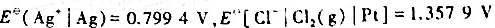 .
.
(1)写出电极反应和电池图示;
(2)求25°C、电池可逆放电2F电荷悬时的热Qz;
(3)求25°C时AgCl的活度积Kap.
第7题
A.氢气在负极发生氧化反应
B.供电时的总反应为:2H2+O2=H2O
C.正极:O2+4eˉ+2H2O=4OHˉ
D.电池在工作一段时间电解质溶液浓度不变
第8题
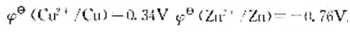 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()A.上升0.24V
B.下降0.24V
C.上升0.12V
D.下降0.12V
第9题
A.温度下降,电极的反应率也随之下降,电流减小
B.温度上升,电极的反应率也随之上升,电流增大,消耗能量
C.冰箱是放电池的好地方
D.锌空电池如果相对湿度太低,电池中的电解质会慢慢变干
E.锌空电池相对湿度太高,系统会存储水分I
第11题
A.它的最小单位称为原电池,是组成电池的重要组件
B.电池可以被当做一个电化学能转换系统,与内燃机类似
C.习惯上把原电池所具有的特性作为电池的特性
D.把化学能转换成机械能,完成这个过程需要两大物质:燃料和氧气
E.其中的一个电极使用金属物质,如锌、锂,在电解质中产生了负电压,代表负电极