 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
要除去FeSO4溶液中少量的CuSO4,宜选用的金属试剂是()
A.铜粉
B.铝粉
C.银粉
D.铁粉
 答案
答案
D、铁粉
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.铜粉
B.铝粉
C.银粉
D.铁粉
 答案
答案
D、铁粉
 更多“要除去FeSO4溶液中少量的CuSO4,宜选用的金属试剂是()”相关的问题
更多“要除去FeSO4溶液中少量的CuSO4,宜选用的金属试剂是()”相关的问题
第1题
A.鉴别软水和硬水——观察颜色
B.鉴别NaOH和NH4NO3两种固体——取样、加水溶解、触摸烧杯外壁
C.除去MnO2中的少量KCl固体——加足量水溶解、过滤、蒸发
D.除去FeSO4溶液中的少量CuSO4——加足量锌粉、充分反应后过滤
第2题
A.除去FeSO4 溶液中含有 CuSO4 杂质,加入足量铁粉,过滤
B.除去NaOH 溶液 中含有Na2CO3 杂质,加入适量 Ca(OH)2 溶液,结晶
C.H2 气体( HCl 气体)依次通过碳酸钠溶液和浓硫酸
D.除去CuO 粉末中含有的碳粉,在空气中充分灼烧
第3题
A.鉴别碳粉、铁粉、氧化铜三种黑色固体:加人稀硫酸,观察现象
B.鉴别NaOH、CuSO4、NaCl三种固体:加水,观察现象
C.除去NaCl溶液中的少量MgCl2 :加入过量的NaOH溶液,过滤
D.除去CaCl2溶液中的少量HCl:加入过量的碳酸钙固体,过滤
第4题
A.用蒸发结晶法除去KNO3中少量的NaCl
B.用加入NaOH(aq)并蒸馏的方法除去乙醛中少量的乙酸
C.准确称取14.800g Ca(OH)2,配制100mL 2.0 mol/L的Ca(OH)2溶液
D.在2mL10%的CuSO4(aq)中滴入3滴 2%的NaOH(aq),配制检验醛基的试剂
第5题
A.向某固体中加入稀盐酸有气泡产生,可证明该物质中一定含有CO
B.常温下可用Fe与AgCl反应制取Ag
C.用过量的Cu(OH)2除去CuSO4溶液中的少量H2SO4
D.可分别将Mg、Fe、Cu、Ag放入稀盐酸中,可确定它们的活动性顺序
第6题
A.KNO3 HCl CuSO4
B.Na2SO4 Zn(NO3)2 H2SO4
C.MgCl2 NaOH FeSO4
D.Na2CO3 Ba(OH)2 K2SO4
第7题
A.向CuCl2溶液中加入CaCO3,调节pH可除去溶液中混有的Fe3+
B.配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度
C.用加热的方法可以除去KCl溶液中的Fe3+
D.洗涤油污常用热的碳酸钠溶液
第8题
B、滤出的不溶物中只有铁,不可能含有铜
C、滤出的不溶物中一定含有铜,也可能含有铁
D、滤液中一定含有FeSO4,也可能含有CuSO4和H2SO4
第10题
从含镍废催化剂中可回收镍,其流程如下: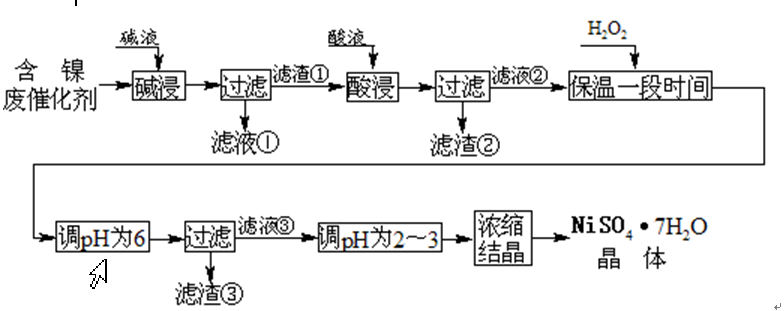 某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
问题一、碱浸“的目的是除去()。
问题二、“酸浸”时所加入的酸是()(填化学式)。酸浸后,滤液②中可能含有的金属离子是()。
问题三、“调pH为2~3”的目的是()。
问题四、产品晶体中有时会混有少量绿矾(FeSO4•7H2O),可能是由于生产过程中()导致Fe2+未被完全氧化造成的。
问题五、NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料——NiOOH。该反应的离子方程式是()
第11题
在CO2气体中混有少量HCl,要除去HCl,最好用()处理。
A.氨水
B.NaHCO3饱和溶液
C.浓硫酸
D.Na2CO3溶液