 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
单质X2和Y2起反应生成化合物的分子式是XY,已知X是正价,下列叙述正确的是()。
A.X2被还原,X2是还原剂
B.Y2被氧化,Y2是氧化剂
C.X2被氧化,X2是还原剂
D.Y2被氧化,Y2是还原剂
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.X2被还原,X2是还原剂
B.Y2被氧化,Y2是氧化剂
C.X2被氧化,X2是还原剂
D.Y2被氧化,Y2是还原剂
 答案
答案
 更多“单质X2和Y2起反应生成化合物的分子式是XY,已知X是正价,下列叙述正确的是()。”相关的问题
更多“单质X2和Y2起反应生成化合物的分子式是XY,已知X是正价,下列叙述正确的是()。”相关的问题
第1题
A.的分子式为C2H4O3
B.的结构简式为HOCH2COOH
C.分子中的官能团有两种
D.与足量的单质Na反应时放出H2的物质的量为0.5mol
第2题
A.单质只含一种元素,所以只含有一种元素的纯净物一定是单质
B.氧化物含有氧元素,所以含有氧元素的物质一定是氧化物
C.酸和碱反应生成盐和水,所以生成盐和水的反应,其反应物一定是酸和碱
D.有机物含有碳元素,所以含有碳元素的化合物一定是有机物
第3题
A.
该反应有单质生成,属于置换反应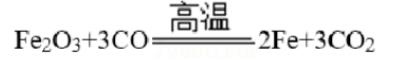
B.
反应后固体质量减少,该反应不遵循质量守恒定律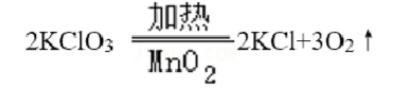
C.化学反应在生成新物质的同时,还伴随着能量的变化
D.化合反应的反应物一定是单质,生成物一定是化合物
第4题
A.正丁烷和异丁烷属于同系物
B.分子式为C2H6O的有机化合物性质相同
C.碳元素的单质只存在金刚石和石墨这两种同素异形体
D.有机化合物CH3—CH2—NO2和H2N—CH2—COOH是同分异构体
第5题
A.微粒观:保持C60化学性质的最小微粒是碳原子
B.元素观:H2O是H、O元素组成的化合物,金刚石和石墨都是碳元素组成的单质
C.变化观:石墨在一定条件下转化为金刚石,属于化学变化
D.守恒观:6gC和16gO2充分反应后,一定生成22gCO2
第6题
推理判断:
(1)将白色固体化合物(A)加热,生成(B)和(C)。白色固体(B)可以溶于稀盐酸生成(D)的溶液,再向其中滴加适量氢氧化钠生成白色沉淀(E),氢氧化钠过量时沉淀消失。(C)是(F)的酸酐,浓酸(F)与单质硫作用生成有刺激性气味的气体化合物(G)和水,稀酸(F)与金属锌作用生成化合物(A)。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(2)向化合物(A)的水溶液中,通入硫化氢气体,生成黑色沉淀(B),(B)经过过氧化氢处理转化成(C)。离心分离后将白色沉淀物(C)加热分解,得到(D)和(E)。(D)与氧化钡反应生成白色固体(F),(F)不溶于水,也不溶于稀硝酸。(E)与稀硝酸反应又生成(A)。(A)受热分解得黄色固体化合物(E),
试给出(A),(B),(C),(D),(E)和(F)的化学式,并完成各步的化学反应方程式。
(3)向化合物(A)的水溶液中,滴加一种钠盐(B)的溶液,先生成白色沉淀(C),(B)的溶液过量时沉淀消失生成(D),继续加入少许盐酸,产生有刺激性气味的气体(E)和黑色沉淀(F),同时体系呈乳白色浑浊状,表示有单质(G)生成。离心分离后固体物质(F)和(C)一同与过量稀硝酸共热,形成的溶液比(A)的溶液多出一种离子(H),因此可以与氯化钡反应生成白色沉淀(I);向清液中加入氯化钡溶液,亦有(I)生成,(I)不溶于稀硝酸。白色沉淀(C)不稳定,与水共存时有(F)和(H)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H)和(I)的化学式,并完成各步的化学反应方程式。
第7题
随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
 根据判断出的元素回答问题:(1)z在周期表中的位置是()。
根据判断出的元素回答问题:(1)z在周期表中的位置是()。
(2)写出x和d组成的一种四原子共价化合物的电子式()。
(3)y、g、h的最高价氧化物对应水化物的酸性最强的是()(填化学式)。
(4)写出f的最高价氧化物与e的最高价氧化物对应的水化物反应的离子方程式()。
(5)己知e和g的最高价氧化物对应的水化物的稀溶液反应生成1mol水时所放出的热量为Qk。请写出该反应的中和热的热化学方程式()。
(6)用y元素的单质与f元素的单质可以制成电极浸入由x、d、e三种元素组成的化合物的溶液中构成电池负极反应式为()。
第8题
A.X的氢化物的沸点一定小于R的氢化物的沸点
B.Q的氮化物溶于盐酸生成两种盐的物质的量之比为1:1
C.Z单质可以从U的钠盐溶液中将其置换出来
D.uSO4溶液能用作T_4中毒的解毒剂
第9题
A.X2为0.2
B.Y2为0.2
C.Z为0.3
D.Z为0
第10题
A.Z为0.3 mol•L-1
B.Y2为0.4 mol•L-1
C.X2为0.2 mol•L-1
D.Z为0.4 mol•L-1
第11题