 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在碱性溶液中用HCHO还原HAuCl4以制备金溶胶,反应可表示为 HAuCl4+5NaOH→NaAuO2+4NaCl+3H2O 2NaAuO2+3HCHO
在碱性溶液中用HCHO还原HAuCl4以制备金溶胶,反应可表示为
HAuCl4+5NaOH→NaAuO2+4NaCl+3H2O
2NaAuO2+3HCHO+NaOH→2Au+3HCOONa+2H2O
此处NaAuO2是稳定剂,试写出胶团结构式,并标出胶核、胶粒和胶团。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在碱性溶液中用HCHO还原HAuCl4以制备金溶胶,反应可表示为
HAuCl4+5NaOH→NaAuO2+4NaCl+3H2O
2NaAuO2+3HCHO+NaOH→2Au+3HCOONa+2H2O
此处NaAuO2是稳定剂,试写出胶团结构式,并标出胶核、胶粒和胶团。
 答案
答案
 更多“在碱性溶液中用HCHO还原HAuCl4以制备金溶胶,反应可表示为 HAuCl4+5NaOH→NaAuO2+4NaCl+3H2O 2NaAuO2+3HCHO”相关的问题
更多“在碱性溶液中用HCHO还原HAuCl4以制备金溶胶,反应可表示为 HAuCl4+5NaOH→NaAuO2+4NaCl+3H2O 2NaAuO2+3HCHO”相关的问题
第1题
A.油脂属于天然高分子化合物
B.热的烧碱溶液去油渍效果更好
C.清洗时,油脂在碱性条件下发生水解反应
D.烧碱具有强腐蚀性,故清洗时必须戴防护手套
第4题
某化合物的分子式为C7H7O2N(A),无碱性,还原后得C7H9N(B)具有碱性。B在低温及强酸存在下,和亚硝酸作用生成C7H7N2Cl(C)。将此化合物C的水溶液加热时,放出N2,并生成对甲基苯酚。在碱性溶液中,化合物C与苯酚作用生成具有颜色的化合物C13H12ON2,请写出A、B、C、D的构造式和各步的反应式。
第5题
从含镍废催化剂中可回收镍,其流程如下: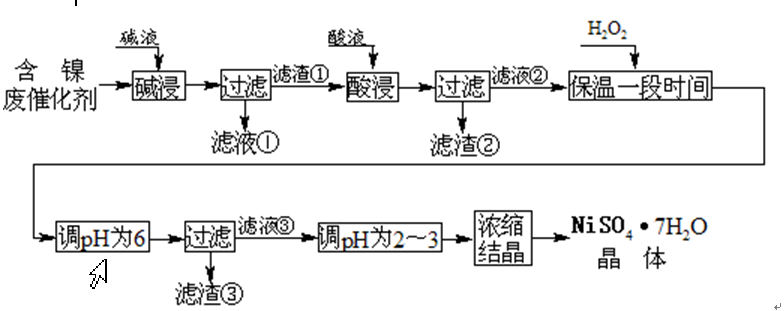 某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
问题一、碱浸“的目的是除去()。
问题二、“酸浸”时所加入的酸是()(填化学式)。酸浸后,滤液②中可能含有的金属离子是()。
问题三、“调pH为2~3”的目的是()。
问题四、产品晶体中有时会混有少量绿矾(FeSO4•7H2O),可能是由于生产过程中()导致Fe2+未被完全氧化造成的。
问题五、NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料——NiOOH。该反应的离子方程式是()
第6题
A.在该反应中碘酸钠作还原剂
B.碱性条件下,氯气的氧化性强于高碘酸钠的氧化性
C.反应中氧化产物与还原产物的物质的量之比为2:1
D.反应中生成1molNa2H3IO6转移2mol电子
第9题
25℃时,向20mL0.1mol/LHAuCl4溶液中滴加0.1mol/LNaOH溶液,滴定曲线如图1所示,含氯微粒的物质的量分数(δ),则下列说法不正确的是()。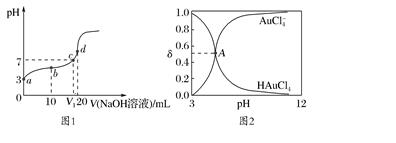
A.图2中A点对应溶液的pH约为5
B.b点对应溶液中:c(Na+)>c(AuCl4﹣)
C.d点对应溶液中:c(OH﹣)﹣c(H+)=c(HAuCl4)
D.滴定过程中,n(HAuCl4)与n(AuCl4﹣)之和保持不变