 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知水的离子积常数 在293 K和303K时分别为 和 .试求:(1) 298 K和标准压力时,中和反应 (1)的
已知水的离子积常数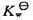 在293 K和303K时分别为
在293 K和303K时分别为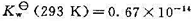 和
和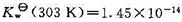 .试求:(1) 298 K和标准压力时,中和反应
.试求:(1) 298 K和标准压力时,中和反应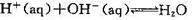 (1)的
(1)的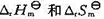 的值(设
的值(设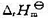 与温度的关系可以忽略);(2) 298 K时OH-的标准摩尔生成Gibbs 自由能
与温度的关系可以忽略);(2) 298 K时OH-的标准摩尔生成Gibbs 自由能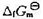 的值。
的值。
已知下述电池的标准电动势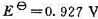 :
:
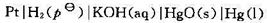
并已知反应 .
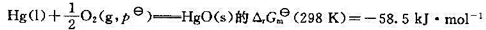
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知水的离子积常数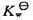 在293 K和303K时分别为
在293 K和303K时分别为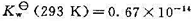 和
和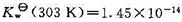 .试求:(1) 298 K和标准压力时,中和反应
.试求:(1) 298 K和标准压力时,中和反应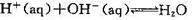 (1)的
(1)的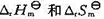 的值(设
的值(设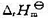 与温度的关系可以忽略);(2) 298 K时OH-的标准摩尔生成Gibbs 自由能
与温度的关系可以忽略);(2) 298 K时OH-的标准摩尔生成Gibbs 自由能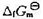 的值。
的值。
已知下述电池的标准电动势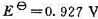 :
:
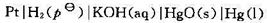
并已知反应 .
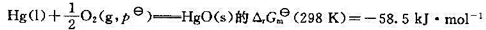
 答案
答案
 更多“已知水的离子积常数 在293 K和303K时分别为 和 .试求:(1) 298 K和标准压力时,中和反应 (1)的”相关的问题
更多“已知水的离子积常数 在293 K和303K时分别为 和 .试求:(1) 298 K和标准压力时,中和反应 (1)的”相关的问题
第1题
A.(H+)随着温度升高而降低
B.在35℃时,c(H+)>c(OH—)
C.水的电离程度:(25℃)>(35℃)
D.水的电离是吸热的
第3题
已知25°C时水的离子积KW=1.008x10-14,NaOH,HCI和NaCl的Amm分别等于0.024811S.m2·mol-1.0.042616S.m2.mol-1和0.012645S.m2.mol-1.
(1)求25°C时纯水的电导率;
(2)利用上述纯水配制AgBr饱和水溶液,测得溶液的电导率k(溶液)=1.664x10-5S.m-1,求AgBr(s)在纯水中的溶解度.
第4题
计算在1,10-邻二氮菲存在下,溶液含H2SO4浓度为1mol.L-1时,Fe3+/Fe2+电对的条件电势。(忽略离子强度的影响。已知在1mol·L-1H2SO4溶液中,亚铁络合物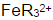 与高铁络合物
与高铁络合物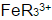 的稳定常数之比KⅡ/KⅢ=2.8×106。)
的稳定常数之比KⅡ/KⅢ=2.8×106。)
第5题
19,有电池Pt|H2(




 H+(
H+(


第6题
A.Na2CO3溶液中c(OH-)大于c(HCO3-)
B.Kw为水的离子积常数,若溶液中c2(OH-)=Kw,溶液pH可能小于7
C.1mol·L-1CH3COOH溶液加水稀释时,溶液中各种离子浓度均减小
D.在CH3COOH溶液中加入碱性固体物质,平衡一定向电离方向移动
第7题
A.升高温度,不可能引起c→b的变化
B.该温度下,水的离子积常数为Kw=10的负14次方
C.该温度下,加入FeCl3可能引起b→a的变化
D.该温度下,稀释溶液可能引起c→d的变化
E.图片如下
第8题
A.=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)=Kw mol·L-1
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
第9题
已知函数f(x)=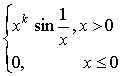 在x=0处连续,则常数k的取值范围为()
在x=0处连续,则常数k的取值范围为()
A.k≤0
B.k>0
C.k>1
D.k>2
第10题
含镉废水通入H2S达到饱和并调整pH值为8.0,请算出水中剩余镉离子的浓度。(已知CdS的溶度积为7.9*10-27,饱和水溶液中H2S浓度保持在0.1mol/L,H2S离解常数K1=8.9*10-8,K2=1.3*10-15)
第11题
在一定条件下,以0.020mol·L-1EDTA溶液滴定等浓度的金属离子M。设其条件稳定常数K'MY=1012,当滴定误差Et=±0.1%时,滴定突跃范围有______个pM单位。