 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298K时,电对MnO4-+8H++5e=Mn2++4H2Oφ0=1.51V,此时H+浓度由1.0mol/L减小至1.0×10-4mol/L,则该电对的电极电势()
A.下降0.047V
B.下降0.38V
C.上升0.047V
D.上升0.38V
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.下降0.047V
B.下降0.38V
C.上升0.047V
D.上升0.38V
 答案
答案
 更多“已知298K时,电对MnO4-+8H++5e=Mn2++4H2Oφ0=1.51V,此时H+浓度由1.0mol”相关的问题
更多“已知298K时,电对MnO4-+8H++5e=Mn2++4H2Oφ0=1.51V,此时H+浓度由1.0mol”相关的问题
第1题
已知298K时,Ca(OH)2(s)的 =-897.5kJ·mol-1,H2O(1)的
=-897.5kJ·mol-1,H2O(1)的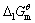 =-237.1kJ·mol-1,
=-237.1kJ·mol-1,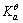 = 1.00×10-7,试求电对Ca(OH)2/Ca的电极电势。
= 1.00×10-7,试求电对Ca(OH)2/Ca的电极电势。
第2题
已知电对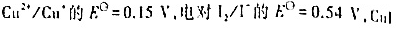 的
的
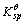 =1.3×10-12。
=1.3×10-12。
(1)试求氧化还原反应
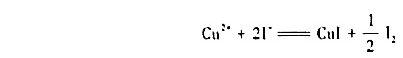
298K时的平衡常数;
(2)若溶液中Cu2+的起始浓度为0.10 mol·dm-3,I-的起始浓度为1.0 mol·dm-3,试计算达到平街时留在溶液中Cu2+的浓度。
第3题
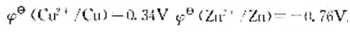 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()A.上升0.24V
B.下降0.24V
C.上升0.12V
D.下降0.12V
第5题
已知下列100kPa,298K时的热力学数据:
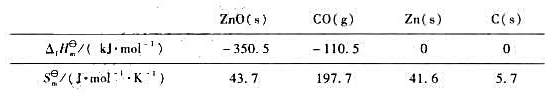
(1)试通过热力学计算,说明下面反应298K时的进行方向:
ZnO(s)+C(s)=Zn(s)+CO(g)
(2)求算上面反应自发正向进行的最低温度。
第6题
已知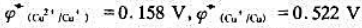 ,请计算反应2Cu+=Cu2++Cu在298K时的反应平衡常数.并由此说明+1价简单Cu+阳离子能否稳定存在于水溶液中?
,请计算反应2Cu+=Cu2++Cu在298K时的反应平衡常数.并由此说明+1价简单Cu+阳离子能否稳定存在于水溶液中?
第7题
2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g)
根据教材附录中的数据。计算反应在298K时的标准摩尔焓变 。若反应的热能完全转化为势能, 可将100kg的重物垂直升高多少?已知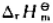 (N2H4,l)=50.63kJ·mol-1.
(N2H4,l)=50.63kJ·mol-1.
第8题
已知 298K,标准状态下
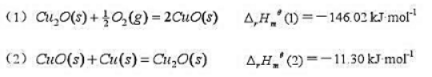
求(3)CuO(s) = Cu(s)+1/2O2(g)的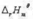
第9题
(1)由附表六中查出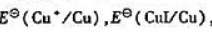 试计算
试计算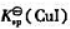 .
.
(2)计算298K下反应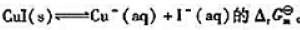
(3)若已知(2)中反应的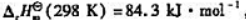 计算该反应的
计算该反应的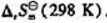
第10题
第11题
298K下,0.2mol·L-1的HAc溶液与0.2mol·L-1的NaAc溶液等体积混合后,该溶液的pH为() , 已知:HAc的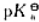 =4.76
=4.76