 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
用理想气体状态方程和压缩因子计算CO2在t=100℃、v=0.012m³/kg时的压力.
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“用理想气体状态方程和压缩因子计算CO2在t=100℃、v=0.012m³/kg时的压力.”相关的问题
更多“用理想气体状态方程和压缩因子计算CO2在t=100℃、v=0.012m³/kg时的压力.”相关的问题
第1题
298.15K,1x10-3m3容器中的压力值,并与用理想气体状态方程计算的压力值进行比较.
第2题
在实际气体状态方程PV=ZRT中Z是压缩因子它是()。
A.一定值
B.随气体的体积变化
C.随温度和压力变化
D.随温度而变化
第4题
已知水(H2O,I)在100℃的饱和蒸气压p=101.325kPa,在此温度.压力下水的摩尔蒸发焓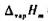 =40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
=40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
第6题
用0.1000mol/LHCl溶液滴定0.1000mol/LNa2CO3溶液至pH5.00。计算有百分之几的Na2CO3变成了H2CO3?剩下的主要组分是什么?如果煮沸溶液以除尽CO2,冷却后溶液的pH为多少?(H2CO3的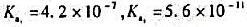 )
)
第7题
第8题
(1)每升碱液吸收了多少克CO2?
(2)用该碱液滴定某一元弱酸,若浓度仍以0.1026ml·L-1计算,会引起多大误差?
第10题
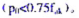
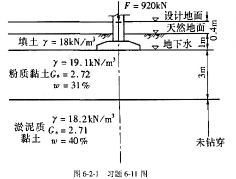
第11题
反应CaCO3(s)——CaO(s)+CO2(g)在973K时 =2.92×10,900℃时 =1.04,试由此计算该反应的
=2.92×10,900℃时 =1.04,试由此计算该反应的 .
.