 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生0.4mol的NO2气体和0.03mol的N2O4气体,在反应后的溶液中加入足量的氢氧化钠溶液,生成沉淀质量为17.02 g。则x等于()
A.8.64
B.9.20
C.9.00
D.9
 答案
答案
B、9.20
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.8.64
B.9.20
C.9.00
D.9
 答案
答案
B、9.20
 更多“取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生0.4mol的NO2气体和0.03mol的N2O4气体,在反应后的溶液中加入足量的氢氧化钠溶液,生成沉淀质量为17.02 g。则x等于()”相关的问题
更多“取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生0.4mol的NO2气体和0.03mol的N2O4气体,在反应后的溶液中加入足量的氢氧化钠溶液,生成沉淀质量为17.02 g。则x等于()”相关的问题
第1题
A.150mL
B.120mL
C.90mL
D.60mL
第2题
推理判断:
(1)将白色固体化合物(A)加热,生成(B)和(C)。白色固体(B)可以溶于稀盐酸生成(D)的溶液,再向其中滴加适量氢氧化钠生成白色沉淀(E),氢氧化钠过量时沉淀消失。(C)是(F)的酸酐,浓酸(F)与单质硫作用生成有刺激性气味的气体化合物(G)和水,稀酸(F)与金属锌作用生成化合物(A)。
试给出(A),(B),(C),(D),(E),(F)和(G)的化学式,并完成各步的化学反应方程式。
(2)向化合物(A)的水溶液中,通入硫化氢气体,生成黑色沉淀(B),(B)经过过氧化氢处理转化成(C)。离心分离后将白色沉淀物(C)加热分解,得到(D)和(E)。(D)与氧化钡反应生成白色固体(F),(F)不溶于水,也不溶于稀硝酸。(E)与稀硝酸反应又生成(A)。(A)受热分解得黄色固体化合物(E),
试给出(A),(B),(C),(D),(E)和(F)的化学式,并完成各步的化学反应方程式。
(3)向化合物(A)的水溶液中,滴加一种钠盐(B)的溶液,先生成白色沉淀(C),(B)的溶液过量时沉淀消失生成(D),继续加入少许盐酸,产生有刺激性气味的气体(E)和黑色沉淀(F),同时体系呈乳白色浑浊状,表示有单质(G)生成。离心分离后固体物质(F)和(C)一同与过量稀硝酸共热,形成的溶液比(A)的溶液多出一种离子(H),因此可以与氯化钡反应生成白色沉淀(I);向清液中加入氯化钡溶液,亦有(I)生成,(I)不溶于稀硝酸。白色沉淀(C)不稳定,与水共存时有(F)和(H)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H)和(I)的化学式,并完成各步的化学反应方程式。
第4题
A.可以用稀硫酸除去烧水壶底部的水垢
B.春蚕到死丝方尽中的“蚕丝”和棉花的主要成分都是纤维,但两者所属营养成分不同
C.因为铁可以和酸反应所以常温下不可以用铁罐贮存浓硝酸和浓硫酸
D.氯化钠和蔗糖溶于水前者属于化学变化,后者属于物理变化
第5题
A.0.01mol
B.0.02 mol
C.0.03 mol
D.0.04 mol
第6题
体(B)与NaOH共熔后溶于水生成绿色溶液(E),在(E)中加适量H2O2则生成黄色溶液(F)。将(F)酸化变为橙色溶液(G),在溶液(G)中加BaCl2溶液,得黄色沉淀(H)。在(G)的浓溶液中加KCl固体,溶解完全后,经蒸发、浓缩、冷却有橙红色晶体(I)析出。(I)受强热得到的固体产物中有(B),同时得到能支持燃烧的气体(J)。试给出(A),(B),(C),(D),(E),(F),(G),(H),(I)和(J)所代表的物质的化学式,并用化学反应方程式表示各过程。
第7题
工业上利用铅浮渣(主要成分是PbO,Pb,含有少量Ag,CaO和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示: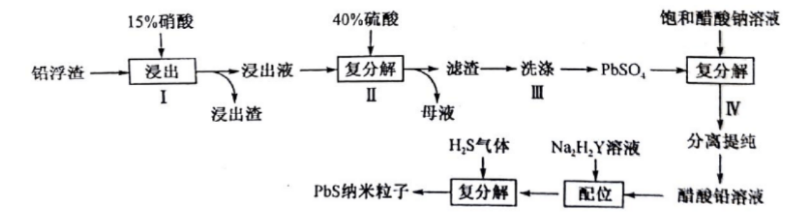 已知:25℃时,
已知:25℃时,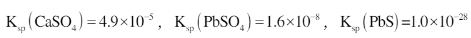 (1)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有()。
(1)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有()。
(2)写出Pb参加反应的化学方程式:()。保持铅剩余的原因是()。
(3)母液的主要成分是()(写化学式),可以循环利用。若母液中残留的SO42-过多,循环利用时可能出现的问题是()。
(4)若浸出液中c(Ca=2+)=0.05mol.L-1,步骤Ⅱ当pb2+完全沉淀后滤渣中是否有CaSO4存在?()(填有或没有)理由是()(通过计算说明)。
第9题
A.不稳定性
B.强氧化性硝酸作为氧化剂时,可以生成一系列的还原产物
C.王水由一体积浓硝酸和三体积的浓盐酸组成的混合酸
D.硝酸盐溶液通常易溶于水溶液酸化后,即可以显示出硝酸的氧化性
第10题