 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在下列物质的工业制法中,生产操作和它的主要目的都正确的是()
A.NaOH:电解槽的阴极产生的是H2,NaOH在阳极附近产生
B.H2SO4:在高温高压下转化SO2,提高转化率和反应速率
C.NH3:氮氢循环操作,提高NH3平衡浓度
D.Na2CO3:分离NaHCO3后的母液中加入食盐,促进NH4Cl结晶
 答案
答案
D、Na2CO3:分离NaHCO3后的母液中加入食盐,促进NH4Cl结晶
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.NaOH:电解槽的阴极产生的是H2,NaOH在阳极附近产生
B.H2SO4:在高温高压下转化SO2,提高转化率和反应速率
C.NH3:氮氢循环操作,提高NH3平衡浓度
D.Na2CO3:分离NaHCO3后的母液中加入食盐,促进NH4Cl结晶
 答案
答案
D、Na2CO3:分离NaHCO3后的母液中加入食盐,促进NH4Cl结晶
 更多“在下列物质的工业制法中,生产操作和它的主要目的都正确的是()”相关的问题
更多“在下列物质的工业制法中,生产操作和它的主要目的都正确的是()”相关的问题
第4题
十二水合硫酸铝钾[KAI(SO4)2・12H2O]俗名明矾,在生活、医药、工业上应用广泛。下面是实脸室探究从铝土矿(主要成分是氧化铝,含少量氧化铁和二氧化硅杂质)制备明矾的流程示意图。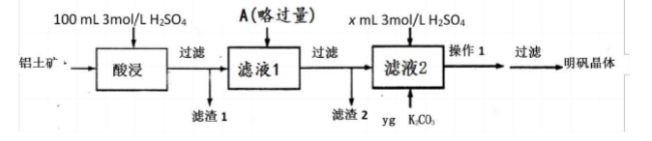 已知:二氧化硅不溶于水,也不与硫酸反应。
已知:二氧化硅不溶于水,也不与硫酸反应。
(1)铝元素在地壳中以()态存在,写出KAl(SO4)·12H2O溶于水的电离方程式()。当明矾溶液中混有NaCl时,简述如何检验Cl()。
(2)滤渣1主要为()(填化学式);以Al2O3为原料,制备该单质铝的反应方程式()。
(3)若A为金属单质,则滤渣2的成分有()。
(4)操作1是蒸发溶剂至有大量晶膜、冷却结晶。实验室进行该操作时,需要的实验仪器有铁架台、()。
(5)如图为某硫酸试剂瓶的标签。若用其配制100mL3mol/L的溶液,需该硫酸()mL(含ρ的表达式)。若此硫酸物质的量浓度为c1,35%的硫酸物质的浓度为c2,则c1()2c2(填大于,小于或等于)。 (6)工业生产中,获取明矾晶体后的母液应该()(填序号)。
(6)工业生产中,获取明矾晶体后的母液应该()(填序号)。
A、弃去
B、返回酸浸流程重复利用
C、返回滤液1重复利用
D、返回滤液2重复利用
第6题
工业上用铝土矿(成分为氧化铝、氧化铁)制取铝的过程如下:
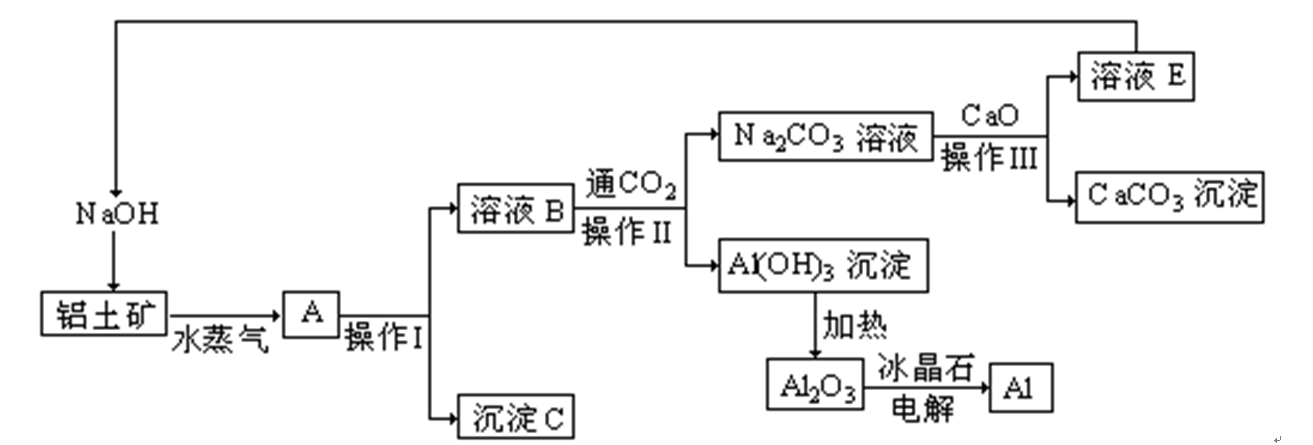 请答复以下问题:
请答复以下问题:
问题一、水蒸气的作用()。
问题二、沉淀C的化学式为(),该物质除了用于金属冶炼以外,还可用作()。
问题三、操作I、操作II、操作III都用到的玻璃仪器是有()。
问题四、实验室洗涤Al(OH)3沉淀应该如何操作:()。
问题五、生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有()(填化学式)。用此法制取铝的副产品是()(填化学式)。
第7题
A.1︰1
B.2︰1
C.1︰2
D.2︰3
第8题
A.1:1
B.2:1
C.1:2
D.2:3
第9题
A.通过仪器来观察世界开阔了人们的视野,由此也改变了我们对物质世界的认识
B.新牌坊立交桥的建成将大大缓解交通高峰期的堵车问题
C.由于适当的温度有助于化学反映速度,工期将选在气温较高的5、6月份
D.这些事故给人民生命财产造成重大损失,究其原因,主要是一些主管领导和管理部门对安全生产没有引起高度重视
第11题
A.物理性质
B.用途
C.制法
D.化学性质