 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
设有1mol的过饱和水蒸气,其温度和压强分别为24℃和1.000bar(1bar=105Pa).当它转化为24℃,0.029824bar的饱和水
设有1mol的过饱和水蒸气,其温度和压强分别为24℃和1.000bar(1bar=105Pa).当它转化为24℃,0.029824bar的饱和水(所谓饱和水是指它的压强恰好是它所在温度的水蒸气的饱和蒸汽压)时,熵的变化是多少?计算时假定可把水蒸气看作理想气体.
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
设有1mol的过饱和水蒸气,其温度和压强分别为24℃和1.000bar(1bar=105Pa).当它转化为24℃,0.029824bar的饱和水(所谓饱和水是指它的压强恰好是它所在温度的水蒸气的饱和蒸汽压)时,熵的变化是多少?计算时假定可把水蒸气看作理想气体.
 答案
答案
 更多“设有1mol的过饱和水蒸气,其温度和压强分别为24℃和1.000bar(1bar=105Pa).当它转化为24℃,0.029824bar的饱和水”相关的问题
更多“设有1mol的过饱和水蒸气,其温度和压强分别为24℃和1.000bar(1bar=105Pa).当它转化为24℃,0.029824bar的饱和水”相关的问题
第1题
1mol氢,在压强为1.0×105Pa,温度为20℃时,其体积为V0。今使它经以下两种过程达同一状态:(1)先保持体积不变,加热使其温度升高到80℃,然后令它作等温膨胀,体积变为原体积的2倍;(2)先使它作等温膨胀至原体积的2倍,然后保持体积不变,加热到80℃。试分别计算以上两种过程中吸收的热量、气体对外做的功和内能的增量;并作出p-V图。
第2题
在100℃和101.325kPa下,1mol水等温蒸发为水蒸气(假设水蒸气为理想气体)。因为此过程中系统的温度不变,所以△U=0,Qp=∫CpdT=0。这一结论是否正确?为什么?
第4题
1mol水在其沸点373.2K时蒸发为水蒸气,求该过程的Q、W、△U、ΔH、ΔS和ΔG,已知该温度下水的气化热为40.67kJ/mol。
第5题
A.气体如果失去了容器的约束就会散开,这是因为气体分子之间存在斥力的缘故
B.一定量的水变成的水蒸气,其分子之间的势能增加
C.对于一定量的气体,如果压强不变,体积增大,那么它一定从外界吸热
D.如果气体分子总数不变,而气体温度升高,气体分子的平均动能增大,因此压强必然增大
第6题
压力为40.53kPa的水汽末态时的△U及△H。设水蒸气可视为理想气体,液体水的体积相对同样物质的量的水蒸气而言可予忽略。
第7题
计算1mol铜在1.013×105Pa压强下温度由300K升到1200K时的熵变。已知在此温度范围内铜的摩尔定压热容为Cp,m=a+bT,其中a=2.3×104J/(mol·K),b=5.92J/(mol·K2)。
第8题
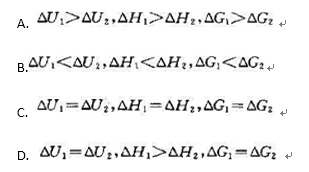
第9题
将一玻璃球放入真空容器中,球中已封入1mol水(101.3kPa、373K),真空容器的容积恰好能容纳1mol的水蒸气(101.3kPa、373K),若保持整个系统的温度为373K,小球被击破后,水全部汽化成水蒸气,汁算Q、W、△U、△H、△S、△G、△A。根据计算结果,这一过程是自发的吗?用哪一个热力学性质作为判据?试说明之。已知水在101.3kPa、373K时的汽化热为40668.5J·mol-1。
第10题
A.饱和汽压跟热力学温度成正比
B.温度一定时,饱和汽的密度为一定值,温度升高,饱和汽的密度增大
C.空气的相对湿度定义为水的饱和汽压与相同温度下空气中所含水蒸气的压强之比
D.空气的相对湿度越大,空气中水蒸气的压强越接近饱和汽压
第11题
此外还有许多副反应,如生成酮、醛及有机酸的反应。反应在温度350℃,压强为0.2026MPa下进行。根据分析,得到反应前后的物料组成(摩尔分数)如下。
组成 | 反应前/% | 反应后/% | 组成 | 反应前/% | 反应后/% |
正丁烷 | 0.63 | 0.61 | 氮 | 27.0 | 26.10 |
正丁烯 | 7.05 | 1.70 | 水蒸气 | 57.44 | 62.07 |
丁二烯 | 0.06 | 4.45 | 一氧化碳 | - | 1.20 |
异丁烷 | 0.50 | 0.48 | 二氧化碳 | - | 1.80 |
异丁烯 | 0.13 | 0 | 有机酸 | - | 0.20 |
正戊烷 | 0.02 | 0.02 | 酮、醛 | - | 0.10 |
氧 | 7.17 | 0.64 |
根据表中的数据计算正丁烯的转化率、丁二烯的收率以及反应的选择性。