 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知电池:Pt,H2()|HAC(1mol·dm-3),NaAc(1mol·dm-3)||KCl(饱和)|Hg2Cl2|Hg,,测得此电池的电动势为0.52V。
已知电池:Pt,H2(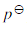 )|HAC(1mol·dm-3),NaAc(1mol·dm-3)||KCl(饱和)|Hg2Cl2|Hg,
)|HAC(1mol·dm-3),NaAc(1mol·dm-3)||KCl(饱和)|Hg2Cl2|Hg,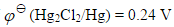 ,测得此电池的电动势为0.52V。
,测得此电池的电动势为0.52V。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知电池:Pt,H2(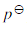 )|HAC(1mol·dm-3),NaAc(1mol·dm-3)||KCl(饱和)|Hg2Cl2|Hg,
)|HAC(1mol·dm-3),NaAc(1mol·dm-3)||KCl(饱和)|Hg2Cl2|Hg,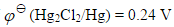 ,测得此电池的电动势为0.52V。
,测得此电池的电动势为0.52V。
 答案
答案
 更多“已知电池:Pt,H2()|HAC(1mol·dm-3),NaAc(1mol·dm-3)||KCl(饱和)|Hg2Cl2|Hg,,测得此电池的电动势为0.52V。”相关的问题
更多“已知电池:Pt,H2()|HAC(1mol·dm-3),NaAc(1mol·dm-3)||KCl(饱和)|Hg2Cl2|Hg,,测得此电池的电动势为0.52V。”相关的问题
第1题
根据以下两个电池求出胃液的pH。
(1)(—)Pt|H2(100kPa)|H+(1.0mol·L-1)||KCl(0.1mol·L-1)|Hg2Cl2(s),Hg()
25℃时测得E=+0.3338V。
(2)(—)Pt|H2(100kPa)|胃液||KCl(0.1mol·L-1)|Hg2Cl2(s),Hg()
25℃时测得E=+0.420V。
第2题
已知溶液中Cd2+和Zn2+浓度均为0.1mol.kg-1,H2在Pt、Cd和Zn上的超电势分别为0.12V、0.48V和0.70V。问25℃时能否用Pt作为电极以电解沉积Cd2+的方法来分离溶液中的Cd2+和Zn2+?已知25℃时,
1.jpg) 假设电解过程中保持溶液的pH=7,析出的H2(g)压力为100kPa。
假设电解过程中保持溶液的pH=7,析出的H2(g)压力为100kPa。
第3题
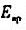 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。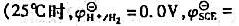
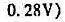
第4题
已知

Cd|Cd2+(0.10mol·L-1)||Sn4+(0.10mol·L-1),Sn2+(0.0010mol·L-1)|Pt在298K时的电动势ε,并写出电池反应,标明正、负极。
第5题
今有原电池如下:
(-)Pt,H2(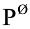 )|HA(0.5mol·L-1)‖NaCl(1mol·L-1)|AgCl(s),Ag()经测定知其电动势为0.568V,试计算一元酸HA的电离常数。[
)|HA(0.5mol·L-1)‖NaCl(1mol·L-1)|AgCl(s),Ag()经测定知其电动势为0.568V,试计算一元酸HA的电离常数。[ (AgCl/Ag)=0.2223V]
(AgCl/Ag)=0.2223V]
第6题
电池Cu|Cu+||Cu+,Cu2+|pt和电池Cu|Cu2+||Cu2+,Cu+|Pt的反应均写成Cu+Cu2+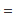 2Cu+,此两电池的( )。
2Cu+,此两电池的( )。

第7题
电池Pt∣Cl2(p1)∣HCl(aq)∣Cl2(p2)∣Pt的电动势E>0,则p1_______p2。
第8题
欲配制pH=3的缓冲溶液,已知有下列物质的Ka数值:
(1) HCOOH Ka=1.77×10-4;
(2) HAc Ka=1.76×10-5;
(3) NH4+Ka=5.65×10-10。
问选择哪一种弱酸及其共轭碱较合适?
第9题
A.4.75
B.6.25
C.7.00
D.9.25
第10题
298K下,0.2mol·L-1的HAc溶液与0.2mol·L-1的NaAc溶液等体积混合后,该溶液的pH为() , 已知:HAc的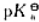 =4.76
=4.76
第11题