 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
水除了能溶解固体和()之外,还能溶解少量的氧气、二氧化碳等()。水中的动物和植物就是靠溶解在水中的()进行呼吸的
A.液体、物质、氧气
B.气体、液体、二氧化碳
C.液体、气体、氧气
 答案
答案
C、液体、气体、氧气
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.液体、物质、氧气
B.气体、液体、二氧化碳
C.液体、气体、氧气
 答案
答案
C、液体、气体、氧气
 更多“水除了能溶解固体和()之外,还能溶解少量的氧气、二氧化碳等()。水中的动物和植物就是靠溶解在水中的()进行呼吸的”相关的问题
更多“水除了能溶解固体和()之外,还能溶解少量的氧气、二氧化碳等()。水中的动物和植物就是靠溶解在水中的()进行呼吸的”相关的问题
第1题
A.鉴别软水和硬水——观察颜色
B.鉴别NaOH和NH4NO3两种固体——取样、加水溶解、触摸烧杯外壁
C.除去MnO2中的少量KCl固体——加足量水溶解、过滤、蒸发
D.除去FeSO4溶液中的少量CuSO4——加足量锌粉、充分反应后过滤
第2题
A.鉴别软水和硬水 观察颜色
B.鉴别NaOH和NH4NO3两种固体 取样、加水溶解、触摸烧杯外壁
C.除去MnO2中的少量KCl固体 加足量水溶解、过滤、蒸发
D.除去FeSO4溶液中的少量CuSO4 加足量锌粉、充分反应后过滤
第3题
A.向20℃时该溶液中加入少量水,溶液变稀
B.取少量溶液降温,有固体析出
C.向20℃时该溶液中加入少量硝酸钾,硝酸钾不再溶解
D.取少量溶液升高温度,无固体析出
第4题
正极材料为LiCoO2的锂离子电池被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
问题一、橄榄石型LiFePO4是一种潜在的锂离子电池正极材料,它可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
①共沉淀反应投料时,不将(NH4)2Fe(SO4)2和LiOH溶液直接混合的原因是()。
②共沉淀反应的化学方程式为()。
③高温成型前,常向LiFePO4中加入少量活性炭黑,其作用除了可以改善成型后的LiFePO4的导电性能外,还能()。
问题二、废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过以下实验方法回收钴、锂 。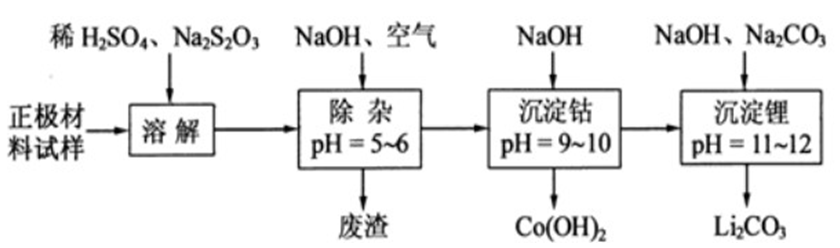
①在上述溶解过程中,S2O32ˉ被氧化成SO42ˉ,LiCoO2在溶解过程中反应的化学方程式为()。
②Co(OH)2在空气中加热时,固体残留率随温度的变化如以下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体成分为()。(填化学式);在350~400℃范围内,剩余固体成分为()。(填化学式) 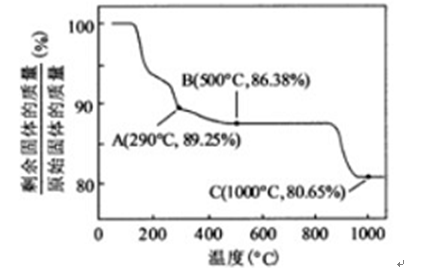
第7题
A.鉴别软水和硬水 实验方案:观察颜色
B.鉴别NaOH和NH4NO3 两种固体 实验方案:取样,加水溶解、触摸烧杯外壁
C.除去MnO2中的少量KCl固体 实验方案:加入适量水溶解、过滤、蒸发
D.除去FeSO4溶液中少量CuSO4 实验方案:加入适量锌粉、充分反应后过滤
第8题
A.蒸发掉5g水有晶体析出
B.降温至10℃时有晶体析出
C.加入少量硝酸钾固体不在溶解
D.先蒸发掉5g水再降温至10℃时有晶体析出
第9题
A.氢氧化钠固体溶于水时吸收热量,溶液温度升高
B.将几滴植物油滴加入汽油中,振荡后可形成乳浊液
C.在硝酸钾饱和溶液中加少量氯化钠固体,氯化钠固体能够溶解
D.稀释浓硫酸时,为防止液体沸腾溅出,应小心将水倒入浓硫酸中
第10题
A.鉴别CaCO3、NaCl和硫酸铜固体: 分别加入适量水观察现象
B.除去KCl溶液中少量K2SO4: 加入适量的BaCl2溶液过滤
C.除去CO2中的把HCl气体: 先通过NaOH溶液,再通过浓硫酸
D.除去碳酸钙中少量的硫酸铜粉末: 加入足量的水溶解、过滤、洗涤干燥
第11题
①用铂丝蘸少量液体在火焰上灼烧,产生黄色火焰。
②它使酸化的KMnO4溶液褪色而产生无色溶液,此溶液与BaCl2溶液作用生成不溶于稀HNO3的白色沉淀。
③加入硫粉,并加热,硫溶解生成无色溶液,此溶液酸化时产生乳白色或浅黄色沉淀,此溶液也能使KI3溶液褪色,并能溶解AgBr。