 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在373K、101.325kPa下,1mol水全部蒸发为水蒸气,求此过程的Q、W、△U和△H。已知水的摩尔气化热为40.
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“在373K、101.325kPa下,1mol水全部蒸发为水蒸气,求此过程的Q、W、△U和△H。已知水的摩尔气化热为40.”相关的问题
更多“在373K、101.325kPa下,1mol水全部蒸发为水蒸气,求此过程的Q、W、△U和△H。已知水的摩尔气化热为40.”相关的问题
第1题
在101.325kPa压力下,若水中只含有直径为10-6m的空气泡,那么这样的水在什么温度下才能沸腾?已知水在373K的表面张力σ=58.9×10-3N/m,摩尔气化热△vapHm=40.656kJ/mol。设水面至空气泡之间液柱的静压力及气泡内蒸汽压下降等因素均可忽略不计。
第2题
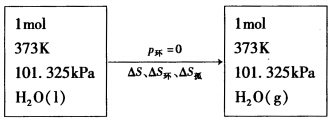
1mol水在373K和101.325kPa向真空蒸发,变成373K和101.325kPa的水蒸气,试计算此过程的△S、△S环、和△S孤,并判断此过程是否自发。
第4题
373K时,水的表面张力为0.0589 N·m-1,密度为958.4kg·m-3。直径为100nm的气泡内(即球形凹面上),在373K时的水蒸气压力为多少?在101.325kPa外压下,能否从373K的水中蒸发出直径为100nm的蒸气泡?
第5题
在373K下,反应:COCl2(g)
 CO(g)+Cl2(g)的K=8×10,△S373=125.5J/K。 计算:(1)373K,总压为202.6kPa时COCl2的解离度; (2)373K下上述反应的△H; (3)总压为202.6kPa,COCl2的解离度为0.1%时的温度,设△Cp=0。
CO(g)+Cl2(g)的K=8×10,△S373=125.5J/K。 计算:(1)373K,总压为202.6kPa时COCl2的解离度; (2)373K下上述反应的△H; (3)总压为202.6kPa,COCl2的解离度为0.1%时的温度,设△Cp=0。
第6题
在101.325kPa、273.15K下,1mol固体冰融化为水时的Q( )0;W( )0;△U( )0(填>、<或=)。
第7题
甲醇(CH3OH)在101.325kPa下的沸点(正常沸点)为64.65℃,在此条件下的摩尔蒸发焓△vapHm=35.32kJ·mol-1。求在上述温度、压力条件下,1kg液态甲醇全部成为甲醇蒸气时的Q,W,△U,△H及△S。
第8题
甲醇(CH3OH)在101.325kPa下的沸点(正常沸点)为64.65℃,在此条件下的摩尔蒸发焓△vapHm=35.32kJ·mol-1。求在上述温度、压力条件下,1kg液态甲醇全部成为甲醇蒸气时的Q,W,△U,△H及△S。
第9题
PCI5的分解反应为: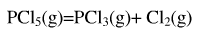 。在523.2K,101.325kPa下反应达到平衡后,测得平衡混合物的密度为2.695×103kg·m-3,试计算:
。在523.2K,101.325kPa下反应达到平衡后,测得平衡混合物的密度为2.695×103kg·m-3,试计算:
(1) PCI5(g)的解离度;(2) 该反应的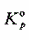 ;(3)该反应的
;(3)该反应的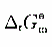 。
。
第10题
在100℃和101.325kPa下,1mol水等温蒸发为水蒸气(假设水蒸气为理想气体)。因为此过程中系统的温度不变,所以△U=0,Qp=∫CpdT=0。这一结论是否正确?为什么?