 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
解释H原子的3s和3p轨道能量相同,而Cl中的3s轨道能量比相应的3p轨道能量低.
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“解释H原子的3s和3p轨道能量相同,而Cl中的3s轨道能量比相应的3p轨道能量低.”相关的问题
更多“解释H原子的3s和3p轨道能量相同,而Cl中的3s轨道能量比相应的3p轨道能量低.”相关的问题
第1题
A.电子在整个分子范围内运动,不再属于某一特定原子
B.反键分子轨道的能量比所有成键分子轨道高,此当反键分子轨道上有电子时,分子不稳定
C.分子轨道是不同原子的原子轨道线性组合面成,杂化轨道是同一原子的原子轨道组合而成
D.只有符合对称性匹配、能量相近和最大重叠原则的原子轨道才能有效地组合成分子轨道
第2题
A.分子中既有振动运动,又有转动运动
B.分子中有些振动能量是简并的
C.分子中有
D.H、O以外的原子存在
E.分子中有些振动能量相互抵消
第3题
A.全段共五句话,第一层应划在第②句与第③句之间。
B.③、④两句从两方面回答了第①句提出的问题。
C.第②句暗示研究太阳能源问题的重要性。
D.第⑤句是从③、④两句引申出来的,并引发了下文。
第4题
一氧化氮(NO)分子被美国《科学》杂志命名为1992年明星分子。在无机化学和生物无机化学中,NO是已得到深入研究的分子之一。
(1)写出基态的价电子组态,并回答下列问题:
(a)N原子和O原子间形成什么形式的化学键?
(b)键级多少?
(c)按原子共价半径估算N-O间的键长,并和实验测定值115pm比较。
(d)分子第一电离能比N2是高还是低?说明原因。比O2又如何?
(e)NO+键级是多少?估计其键长。
(D)NO+的伸缩振动波数比NO是大还是小?估计其数值.
(2)若忽略电子的轨道运动对磁矩的贡献,计算NO分子的磁矩。
(3)已知NO红外光谱的两个谱带的波数分别为1876.2cm-1和3724.6cm-1,计算第三泛音带的波数。
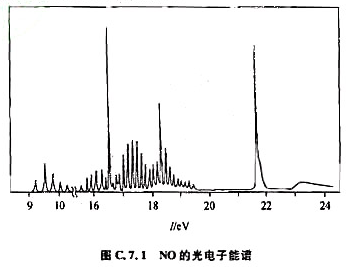
(4)NO紫外光电子能谱(HeⅡ线,40.8eV)的一部分示于图C.7.1中,图中的谱带对应于2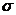 轨道。试解释此能谐分裂为两个谱带(分别对应于3Ⅱ和1Ⅱ态)的原因,并估算从2
轨道。试解释此能谐分裂为两个谱带(分别对应于3Ⅱ和1Ⅱ态)的原因,并估算从2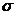 轨道击出的光电子的最大动能。
轨道击出的光电子的最大动能。
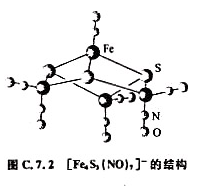
(5)在腌肉时加入NaNO2,产生NO,NO与从蛋白质中解离出来的硫和铁结合生成[Fe4S3(NO)7]-,该离子有抑菌、防腐作用。X射线结构分析表明该离子的结构如图C.7.2所示,请指明该离子所属点群。
第5题
块,每块的质量为m/2。刚爆炸后的两碎块的径向速度分量等于v0/2,其中v0是卫星于爆炸前的轨道速率;在卫星参考系中两碎块在爆炸的瞬间表现为沿着卫星到地心的连接线分离。
(1)用G、M、m和r表示出每一碎块的能量和角动量(以地心系为参考系)。
(2)画一草图说明原来的圆轨道和两碎块的轨道。作图时,利用卫星椭圆轨道的长轴与总能量成反比这一事实。
第6题
第8题
第9题
A.任何提炼乙醇的原料的价格都随季节波动,而提炼的费用则相对稳定
B.燃烧甘蔗废料可提供向乙醇转化所需的能量,而用玉米提炼乙醇则完全需额外提供能源
C.玉米质量对乙醇产出品的影响较甘蔗小
D.用甘蔗制糖或其他食品的生产时间比提炼乙醇的时间长
第10题
由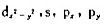 轨道组成dsp2等性杂化轨道
轨道组成dsp2等性杂化轨道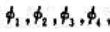 ,这些轨道极大值方向按平面四方形分别和x,y轴平行。根据原子轨道正交、归一性推出各个杂化轨道的d,s,px,py,的组合系数,验证它们是正交、归一的。
,这些轨道极大值方向按平面四方形分别和x,y轴平行。根据原子轨道正交、归一性推出各个杂化轨道的d,s,px,py,的组合系数,验证它们是正交、归一的。